








《九年级化学·课题3 溶液的浓度PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为1.49 MB,总共有21页,格式为ppt。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 21页
- 1.49 MB
- VIP模板
- ppt
- 数字产品不支持退货
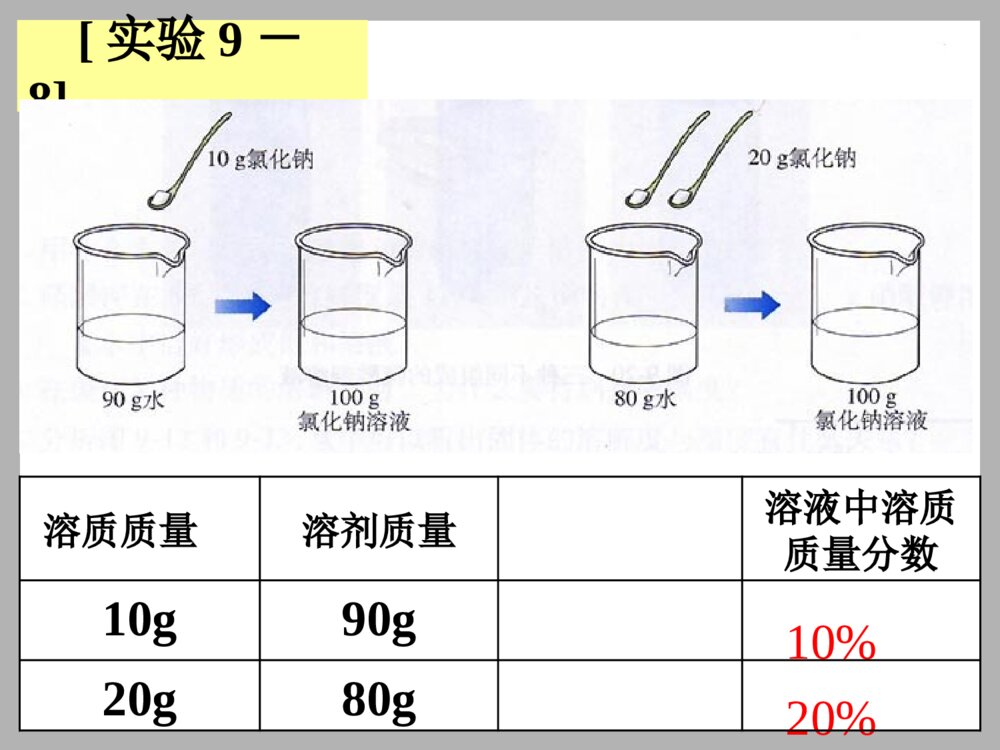
课题3溶液的浓度演示实验9-5颜色:淡蓝蓝色深蓝分析实验结论①对于有色溶液,我们可以根据颜色深浅来判断溶液是浓还是稀;但是这种分法比较粗略,不能准确地表明一定量溶液里究竟含有多少溶质。②在实际应用中,常常要准确知道一定量溶液里含有多少溶质,即溶液的浓度(浓稀程度)。③表示溶液浓度(浓稀程度)的方法很多,今天我们学习:溶质的质量分数药液太稀不能杀死害虫和病菌,但药液太浓又会毒害农作物或树木。喷洒农药课题3溶质的质量分数一、溶质的质量分数1、概念:溶质质量与溶液质量之比。2计算公式:溶质质量溶液质量溶质的质量分数100%溶质质量溶质质量+溶剂质量100%[实验9-8]10%20%溶质质量溶剂质量溶液中溶质质量分数10g90g20g80g[讨论]某氯化钠溶液中溶质的质量分数为10%,其含义是什么?表示100份质量的氯化钠溶液中含有10份质量的氯化钠,90份质量的水。溶质质量:溶剂质量=1:9例1在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150Kg这种溶液,需要氯化钠和水的质量各是多少?解:溶质质量溶液质量溶质的质量分数100%溶质质量溶液质量溶质的质量分数150Kg16%24Kg溶剂质量溶液质量溶质质量150Kg24Kg126Kg练习一配制50g质量分数为5%的氯化钠溶液,需要氯化钠多少克?水多少克?练习二:配制100ml质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3)需要氢氧化钠和水的质量各多少?练习1:将15克食盐放入135克水中完全溶解后(1)所得溶液中溶质的质量分数为.(2)把此溶液分为三等份,每份溶液中溶质的质量分数分别为...(3)在1份溶液中加入5克氯化钠完全溶解后所得溶液中溶质的质量分数为.(4)在另一份溶液中加入10克水后所得溶液中溶质的质量分数为.(5)将第三份溶液加热蒸发掉10克水所得溶液中溶质的质量分数为.10%10%10%10%12.5%8%18.2%讨论:已知20℃时,氯化钠的溶解度是36g。有人说:“20℃时氯化钠饱和溶液中溶质的质量分数为36%。”这种说法对吗?为什么?分析:溶解度氯化钠(溶质)水(溶剂)饱和溶液溶质的质量分数36g36g100g136g26.5%饱和溶液的溶质质量分数=溶解度100g+溶解度结论:练习1、20℃时NaCl的溶解度为36克/100克水,则在20℃时不可能配制的NaCl溶液()A28%B20%C10%D25%2:C的饱和溶液溶质的质量分数为20%,则此时C的溶解度为?例题2:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液需要多少克水?解:设加入水的质量为x50g×98%=(50+X)g×20%答:需要水的质量195g加水前加水后M浓液x1%M稀液x2%50g98%M稀液=M浓液+水加入水xg(50+x)g98%X=195g分析:练习3:用25%的氯化钠溶液和水配制30kg10%的食盐溶液。需要25%的氯化钠溶液和水各多少kg4:某工厂化验室配制5000g20%的盐酸,需要38%的盐酸和水各多少克?5:要配制20%的食盐溶液100g,需要10%和50%的食盐溶液各多少克?注意点:溶液是混合物,溶液的质量不能直接代入化学方程式中计算,必须换算成溶质的质量。例题4:100g9.8%硫酸跟多少克锌反应?同时生成多少克氢气?解:100g9.8%硫酸中含纯硫酸的质量为:100g9.8%=9.8g设参加反应的锌质量为X,生成氢气的质量为YZn+H2SO4=ZnSO4+H265982X9.8gYX=6.5gY=0.2g答:略[[题型四题型四]]::有关化学方程式的计算有关化学方程式的计算练习1:200g稀硫酸恰好和26g锌完全反应。求生成氢气的质量?该稀硫酸溶质的质量分数?2:26g黄铜(Cu-Zn合金)与100g稀硫酸在烧杯中恰好完全反应,反应后测得烧杯中剩余物的总质量为125.8克。求:⑴黄铜中铜的质量分数;⑵稀硫酸溶液中溶质质量分数。(3)硫酸锌质量分数为多少?(提示:反应前后总质量变少的原因是有氢气产生)310g铜锌合金与100g稀盐酸恰好完全反应,烧杯内剩余物质的总质量为109.8g,求:①合金中铜的质量分数②所用稀盐酸的浓度③所得溶液的溶质质量分数4某同学为测定石灰石的纯度,将12g样品放入烧杯中,向其中逐滴滴加7.3%的盐酸,至不再产生气体为止,共用去100g盐酸(杂质不溶于水,也不与水反应),求:①石灰石样品的纯度(即样品中CaCO3的质量分数)②所得混合物中溶液总质量(3)反应后溶液中溶质质量分数?4. 右图是某输液瓶标签上的部分内容。由此可知,葡萄糖由()种元素组成,其中碳元素的质量分数为()。要把10g这种葡萄糖溶液稀释为2%的溶液,需要水的质量为()g。配制溶质质量分数一定的溶液如何配制50g质量分数为6%的氯化钠溶液1、计算:配制时所需NaCl质量为__________,所需水的质量_____,2、称量用托盘天平称3gNaCl固体,倒入烧杯中用50mL量筒量取47mL水,倒入盛有NaCl的烧杯中3、溶解:用玻璃棒搅拌,使NaCl全部溶解4、把配好的溶液装入细口瓶瓶中,盖好瓶塞并贴上标签。(药品名称和溶质的质量分数)3g47g相当于47mL用用固体固体配制一定溶质质量分数的溶液配制一定溶质质量分数的溶液主要仪器:主要仪器:托盘天平、烧杯、量筒、玻璃棒、托盘天平、烧杯、量筒、玻璃棒、药匙、胶头滴管药匙、胶头滴管实验步骤:实验步骤:①①计算计算;;②称量②称量;;③③溶解溶解;;④装瓶,贴标签。练习:下面是一位同学配制一定溶质质量分数的氯化钠溶液时的流程图,请找出其中的错误,并说明理由。



















